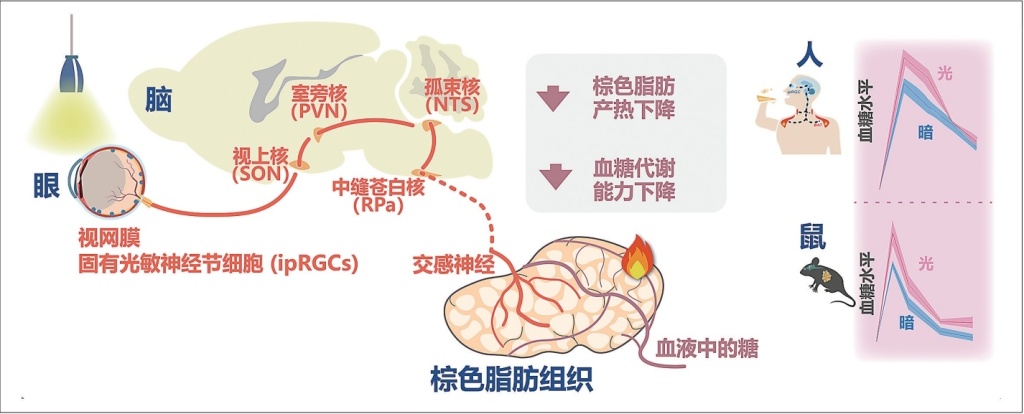
“眼—脑—棕色脂肪轴”介导光调节血糖代谢神经机制示意图。(作者供图)
生命体是在太阳辐照下历经数亿年演化而来,并发展为精确而复杂的调控网络,用以动态响应外界环境,调节身体葡萄糖代谢。这种调控网络在生命历程中发挥着关键作用,以确保生物体能适应不断变化的环境条件。而光如何调控葡萄糖代谢机制仍然是一个待解答的问题,包括解析这一过程中的感光细胞类型、大脑神经联系,以及外周效应器官。
为了研究光调控哺乳动物葡萄糖代谢过程,我们的研究团队进行了葡萄糖耐受性测试,分别在夜行性的小鼠和昼行性的人类中进行。尽管人与小鼠在昼夜生理过程中表现出相反的现象,但我们的研究团队发现,在经历数小时光暴露后,人和小鼠的葡萄糖耐受性都显著降低。这一现象不仅存在于白天,黑夜也如此。然而,这一生理现象的“光感受过程”具体发生在哪里?
哺乳动物的光感受主要始于视网膜上的三类感光细胞,它们在感知环境中不同波长范围的光线方面发挥着关键作用,并调控诸多生理功能。视锥细胞和视杆细胞感知环境光线负责图像认知的成像视觉功能。然而,视网膜中还存在第三类感光细胞,即视网膜自感光神经节细胞(ipRGCs),与大脑中诸多脑区存在神经联系,调控生物钟、睡眠觉醒、情绪变化和认知等非成像视觉功能。
对于哪类感光细胞影响介导糖代谢耐受性问题,我们的研究团队通过基因工程手段构建了分别丧失视锥细胞、视杆细胞和ipRGCs感光能力的转基因小鼠,经葡萄糖耐受性测试发现仅在ipRGCs丧失感光能力的小鼠中,光不再抑制葡萄糖代谢耐受性,这说明光对糖代谢抑制是由ipRGCs感光独立介导的。
在大脑的下丘脑中与ipRGCs有密集连接的核团,包括下丘脑视交叉上核(SCN)和视上核(SON)核团。有研究表明,光照模式改变可以通过影响节律中枢SCN,导致生物钟节律紊乱,从而间接影响葡萄糖代谢功能。
我们的研究团队发现,光降低葡萄糖耐受性的过程与生物钟节律系统无关,揭示了脑内非节律系统神经参与了光对血糖代谢调节。
机体对血液中葡萄糖的利用,很大一部分需要通过外周代谢器官来参与。我们的研究团队发现,中缝苍白核是介导该现象的重要节点。该核团是调节棕色脂肪组织活性的交感前运动神经元聚集区,而棕色脂肪组织是一个重要的代谢器官,其主要作用之一是直接消耗葡萄糖产生热量以维持体温稳态。
研究结果显示,光能显著降低棕色脂肪组织的产热活动。这一发现揭示了光通过神经联系调控棕色脂肪组织活性,导致葡萄糖代谢能力下降。
在志愿者中,我们的研究团队进行了类似的研究,让他们处于29℃的热中性温度条件下,此时棕色脂肪组织活性被显著压抑。结果显示,光在这种条件下不再抑制志愿者的葡萄糖耐受性,表明光降低人体葡萄糖耐受性可能同样是通过影响脂肪组织的活性来介导。
对人体研究结果显示,昼夜节律会造成夜间人体糖代谢能力相较白天更低,在夜间有光暴露的条件下人体血糖代谢能力最差。
在工业化社会中,人类长时间夜晚暴露于人造光源之下,加上夜间饮食习惯给机体带来双重代谢负担,进而可能诱发代谢疾病。
(作者:薛天系中国科学技术大学生命科学与医学部教授,孟建军系中国科学技术大学合肥微尺度物质科学国家研究中心副研究员,沈嘉伟系中国科学技术大学合肥微尺度物质科学国家研究中心博士后研究员)
责任编辑:胡惠雯